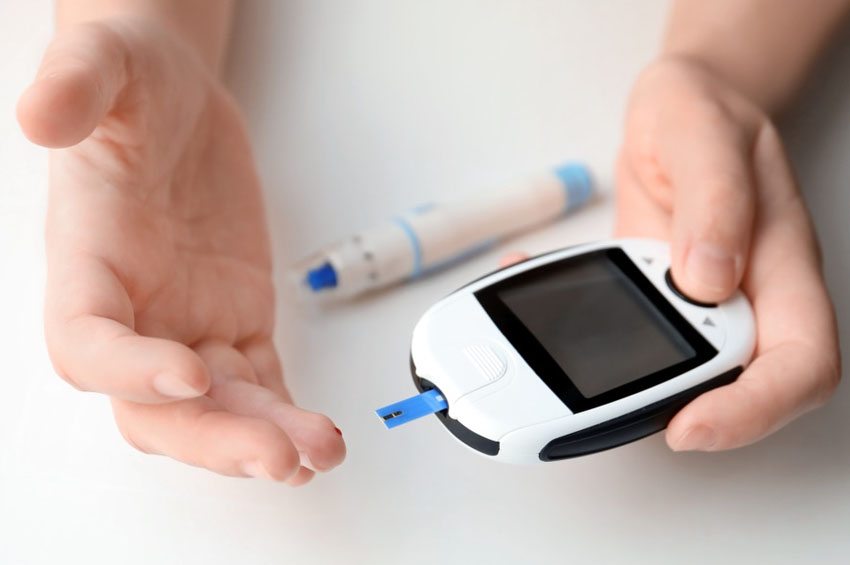
Bir zamanlar erişkin başlangıçlı diyabet olarak adlandırılan tip 2 diyabet, vücudun insülini doğru şekilde kullanamaması ve kanda şeker birikmesiyle ortaya çıkan bir sağlık sorunudur.
Haber Merkezi / Tip 2 diyabet genellikle bir yaşam tarzı hastalığı olarak sınıflandırılır. Bunun nedeni, sağlıksız yaşam tarzı alışkanlıklarıyla bağlantılı insülin direncinden kaynaklanmasıdır.
Tip 2 diyabet, kronik bir durumdur ve şu anki tıbbi bilgilerle tamamen “kür” edilemez, ancak uygun tedavi ve yaşam tarzı değişiklikleriyle etkili bir şekilde yönetilebilir, semptomlar kontrol altına alınabilir ve hatta bazı durumlarda remisyona (hastalık belirtilerinin ortadan kalkması) ulaşılabilir.
İşte detaylar:
Tip 2 Diyabetin Tedavisi: Tedavinin amacı kan şekeri seviyelerini normal aralıkta tutmak, komplikasyonları önlemek ve yaşam kalitesini artırmaktır. Tedavi, yaşam tarzı değişiklikleri ve gerektiğinde ilaç veya insülin tedavisini içerir:
Yaşam Tarzı Değişiklikleri:
Sağlıklı Beslenme:
Düşük glisemik indeksli gıdalar (tam tahıllar, sebzeler, baklagiller) tercih edilmelidir.
Şeker ve işlenmiş karbonhidrat tüketimi sınırlandırılmalı.
Porsiyon kontrolü ve dengeli beslenme (protein, sağlıklı yağlar, lifli gıdalar) önemlidir.
Fiziksel Aktivite:
Haftada en az 150 dakika orta yoğunlukta aerobik egzersiz (yürüyüş, bisiklet, yüzme).
Direnç egzersizleri (ağırlık kaldırma) insülin duyarlılığını artırabilir.
Kilo Kontrolü: Fazla kilolu hastalarda %5-10 oranında kilo kaybı, kan şekeri kontrolünü önemli ölçüde iyileştirebilir.
Stres Yönetimi: Stres, kan şekerini yükseltebilir. Yoga, meditasyon veya rahatlama teknikleri faydalı olabilir.
Sigara ve Alkol: Sigarayı bırakmak ve alkolü sınırlamak komplikasyon riskini azaltır.
İlaç Tedavisi:
Yaşam tarzı değişiklikleri yeterli olmadığında doktorlar ilaç reçete edebilir:
Metformin: İlk tercih edilen ilaçtır; karaciğerde glikoz üretimini azaltır ve insülin duyarlılığını artırır.
Sülfonilüreler: Pankreastan insülin salınımını artırır.
DPP-4 İnhibitörleri, GLP-1 Reseptör Agonistleri: Kan şekeri kontrolünü destekler.
SGLT-2 İnhibitörleri: Böbreklerden glikoz atılımını artırır.
Tiyazolidindionlar: İnsülin duyarlılığını iyileştirir.
İnsülin Tedavisi:
İlaçlarla kan şekeri kontrol altına alınamazsa insülin enjeksiyonları gerekebilir.
Farklı insülin türleri (hızlı etkili, uzun etkili) bireysel ihtiyaca göre kullanılır.
Cerrahi Seçenekler:
Obeziteyle ilişkili Tip 2 diyabet vakalarında bariatrik cerrahi (mide küçültme gibi) kan şekeri kontrolünü iyileştirebilir ve bazı hastalarda remisyona yol açabilir.
Tip 2 Diyabetin Remisyonu Mümkün mü?
Remisyon, kan şekeri seviyelerinin ilaçsız olarak normal aralığa dönmesi ve HbA1c’nin yüzde 6.5’in altında olması durumudur.
Nasıl Sağlanır?:
Önemli kilo kaybı (özellikle hastalığın erken evrelerinde).
Düşük kalorili diyetler veya çok düşük karbonhidratlı (ketojenik) diyetler bazı hastalarda etkili olabilir.
Düzenli egzersiz ve disiplinli yaşam tarzı değişiklikleri.
Not: Remisyon, hastalığın tamamen ortadan kalktığı anlamına gelmez; yaşam tarzı değişiklikleri sürdürülmezse hastalık geri dönebilir.
Komplikasyonların Önlenmesi:
Tip 2 diyabet iyi yönetilmezse kalp hastalığı, böbrek hasarı, sinir hasarı, göz problemleri ve ayak yaraları gibi komplikasyonlara yol açabilir. Bu nedenle:
Kan şekeri, kan basıncı ve kolesterol düzenli izlenmeli.
Yıllık göz, böbrek ve ayak muayeneleri yapılmalı.
Tedavi Mümkün mü?
Tam kür: Günümüz tıbbında Tip 2 diyabetin tamamen ortadan kaldırılması mümkün değildir, çünkü genetik yatkınlık ve pankreas fonksiyonlarındaki değişiklikler kalıcı olabilir.
Yönetim ve Remisyon: Ancak, erken teşhis, yaşam tarzı değişiklikleri ve uygun tedaviyle hastalık kontrol altına alınabilir ve bazı hastalarda ilaç ihtiyacı ortadan kalkabilir.